La (S)-isosérine 15a (21 g, 0,20 mole) a été dissoute dans du tétrahydrofurane (100 ml) et un solvant mixte composé d'une solution aqueuse d'hydroxyde de sodium à 10 % (100 ml) et de dicarbonate de di-tert-butyle (50 ml, 0,22 mole) a été ajouté goutte à goutte. La réaction a été réalisée à température ambiante pendant 9 heures. La phase aqueuse a été ajustée à pH 2 avec 4 mol/L d'acide chlorhydrique et extraite avec du dichlorométhane/méthanol (v/v = 5/1, 50 mL × 3 ) et séché sur sulfate de sodium anhydre. Filtrer par aspiration, concentrer sous pression réduite. Le composé du titre 15b a été obtenu sous la forme d'une huile incolore (35 g, rendement : 85 pour cent).
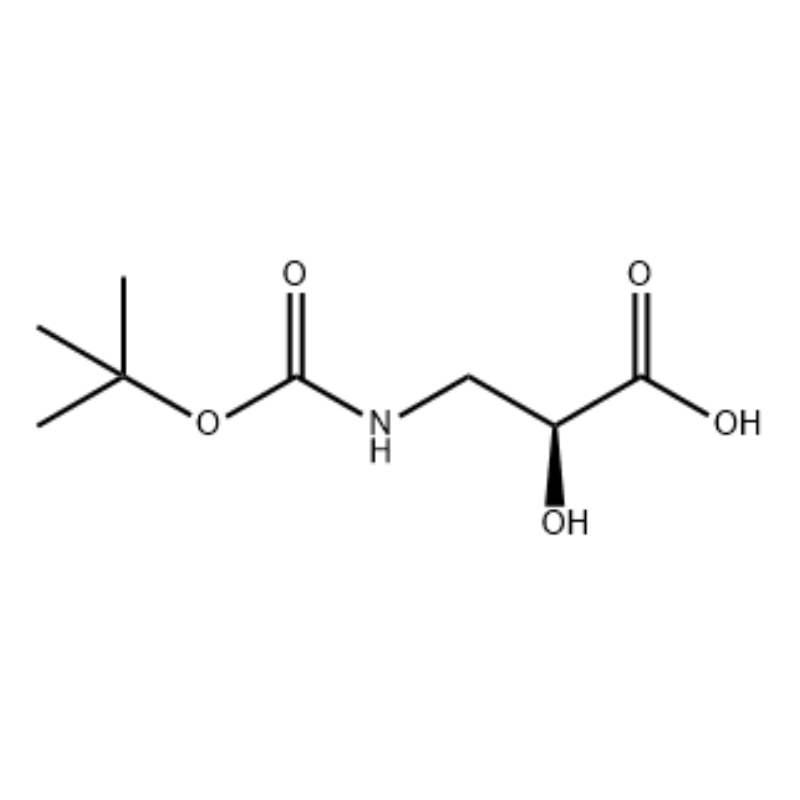
À une solution sous agitation de S-isosérine (4,0 g, 0,038 mol) dans du dioxane : H2O (100 ml, 1:1 v/v) à 0°C a été ajouté de la N-méthylmorpholine (4,77 ml, 0,043 mol), suivie de BoC2O. (11,28 ml, 0,049 mol) et la réaction a été agitée pendant une nuit avec réchauffement progressif jusqu'à température ambiante.De la glycine (1,0 g, 0,013 mol) a ensuite été ajoutée et la réaction a été agitée pendant 20 min.La réaction a été refroidie à 0°C et saturée en solution aqueuse.Du NaHC03 (75 ml) a été ajouté.La couche aqueuse a été lavée avec de l'acétate d'éthyle (2 x 60 ml) puis acidifiée à pH 1 avec NaHSO4.Cette solution a ensuite été extraite avec de l'acétate d'éthyle (3 x 70 ml) et ces couches organiques combinées ont été séchées sur Na2SO4, filtrées et concentrées à sec pour donner l'acide N-Boc-3-ammo-2(S)-hydroxy-propanoïque souhaité. (6,30 g, 0,031 mmol, rendement de 81,5 %) : RMN 1H (400 MHz, CDC13) δ 7,45 (bs, 1 H), 5,28 (bs, 1 H), 4,26 (m, 1 H), 3,40-3,62 (m , 2H), 2,09 (s, 1H), 1,42 (s, 9H);RMN 13C (IOO MHz, CDC13) δ 174,72, 158,17, 82, 71,85, 44,28, 28,45.
Acide N-Boc-3-amino-2(S)-hydroxy-propionique ;À une solution sous agitation de S-isosérine (4,0 g, 0,038 mol) dans du dioxane : H2O (100 ml, 1 : 1 v/v) à 0 ° C a été ajouté de la N-méthylmorpholine (4,77 ml, 0,043 mol), suivie de BoC2O. (11,28 ml, 0,049 mol) et la réaction a été agitée pendant une nuit avec réchauffement progressif jusqu'à température ambiante.De la glycine (1,0 g, 0,013 mol) a ensuite été ajoutée et la réaction a été agitée pendant 20 min.La réaction a été refroidie à 0 °C et saturée en solution aqueuse.Du NaHC03 (75 ml) a été ajouté.La couche aqueuse a été lavée avec de l'acétate d'éthyle (2 x 60 ml) puis acidifiée à pH 1 avec NaHSO4.Cette solution a ensuite été extraite avec de l'acétate d'éthyle (3 x 70 ml) et ces couches organiques combinées ont été séchées sur Na2SO4, filtrées et concentrées à sec pour donner l'acide N-Boc-3-amino-2(5)-hydroxy-propanoïque souhaité. (6,30 g, 0,031 mmol, rendement de 81,5 %) : RMN 1H (400 MHz, CDC13) δ 7,45 (bs, 1 H), 5,28 (bs, 1 H), 4,26 (m, 1 H), 3,40-3,62 (m , 2H), 2,09 (s, 1H), 1,42 (s, 9H);RMN 13C (100 MHz, CDC13) δ 174,72, 158,17, 82, 71,85, 44,28, 28,45.
 Bâtiment 12, n° 309, 2e route sud, zone de développement économique, district de Longquanyi, Chengdu, Sichuan, Chine.
Bâtiment 12, n° 309, 2e route sud, zone de développement économique, district de Longquanyi, Chengdu, Sichuan, Chine. amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com
amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com +86 (028) 84841969
+86 (028) 84841969 +86 135 5885 5404
+86 135 5885 5404

















.png)


